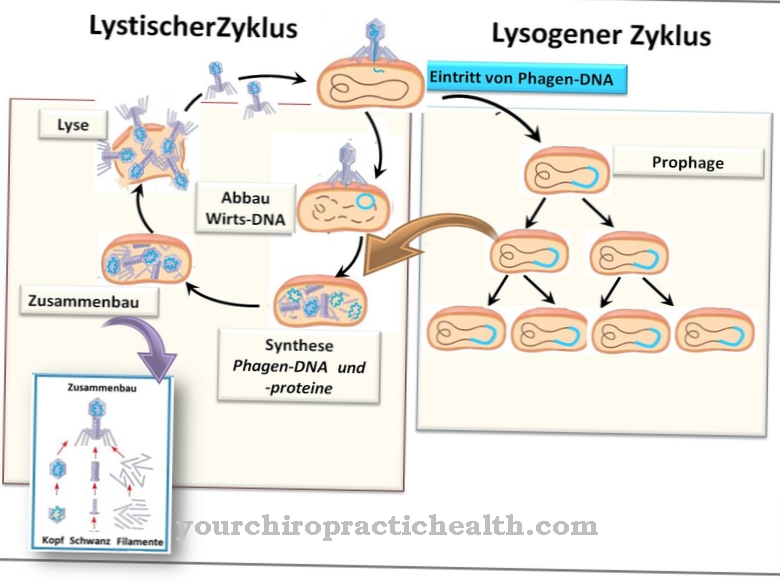
A splice kritikus folyamatot képvisel az eukarióta magjában történő transzkripció során, amelynek során az érett mRNS kilép az pre-mRNS-ből. A transzkripció után még az pre-mRNS-ben lévő intronokat eltávolítjuk, és a fennmaradó exoneket egyesítjük, hogy a kész mRNS-t képezzük.
Mi splicing

A molekuláris biológia központi dogmája kimondja, hogy a genetikai információ áramlása az információhordozó DNS-től az RNS-en keresztül a fehérjéig zajlik. A gén expressziójának első lépése az úgynevezett transzkripció. Az RNS-t a DNS mint templát felhasználásával szintetizáljuk. A DNS a genetikai információ hordozója, amelyet ott tárol egy kód, amely a négy bázis adenből, a timinből, a guaninból és a citozinból áll. Az RNS polimeráz fehérjekomplex leolvassa a DNS alapszekvenciáját a transzkripció során, és előállítja a megfelelő „pre-messenger RNS-t” (rövid ideig pre-mRNS-t). A timin helyett az uracil mindig be van építve.
A gének exonokból és intronokból állnak. Az exonok a genom azon részei, amelyek valójában genetikai információt kódolnak. Az intronok ezzel szemben egy gén nem kódoló szakaszát képviselik: A DNS-en tárolt géneket olyan hosszú szakaszok hajtják át, amelyek nem felelnek meg a későbbi fehérje aminosavainak és nem járulnak hozzá a transzlációhoz.
Egy gén legfeljebb 60 intront tartalmazhat, hossza 35 és 100 000 nukleotid között lehet. Ezek az intronok átlagosan tízszer hosszabbak, mint az exonok. A transzkripció első lépésében előállított pre-mRNS, amelyet gyakran éretlen mRNS-nek is neveznek, még mindig tartalmaz mind exont, mind intront. Itt kezdődik az összeillesztési folyamat.
Az intronokat el kell távolítani az pre-mRNS-ből, és a fennmaradó exonokat össze kell kapcsolni. Csak azután az érett mRNS elhagyhatja a sejtmagot, és kezdeményezheti a transzlációt.
Az összeillesztést nagyrészt a spliceoszóma (német: spliceosome) segítségével végezzük. Ez öt snRNP-ből (kis nukleáris ribonukleoprotein részecskékből) áll. Ezen snRNP-k mindegyike snRNS-ből és fehérjékből áll. Néhány más protein, amely nem része az snRNP-knek, szintén a spliceoszóma részei. A spiceoszómákat nagyobb és kisebb spliciceoszómákra osztjuk. A fő spliciceoszóma az összes humán intron 95% -át meghaladja, a kisebb spliciceoszóma főként az ATAC intront kezeli.
A kötés magyarázatáért Richard John Roberts és Phillip A. Sharp 1993-ban Nobel-díjat kapott az orvostudományban. Thomas R. Cech és Sidney Altman 1989-ben a kémiai Nobel-díjat kapott az alternatív illesztésekkel és az RNS katalitikus hatásával kapcsolatos kutatásaikért.
Funkció és feladat
Az illesztési folyamat során az egyes részekből újból kialakul a spliciceoszóma. Emlősökben az snRNP U1 először az 5'-illesztési helyhez kapcsolódik, és megindítja a fennmaradó spliciceoszóma kialakulását. Az snRNP U2 az intron elágazási pontjához kötődik. Ezután a tri-snRNP-t is megköti.
A spliciceoszóma az összekapcsolási reakciót két egymást követő átészterezéssel katalizálja. A reakció első részében az "ágpont-szekvencia" (BPS) adenozin 2'-OH csoportjának oxigénatomja megtámadja az 5'-illesztési hely foszfodiészter-kötésének foszfor-atomját. Ez felszabadítja az 5 'exont és keringteti az intront. Az 5'-exon most szabad 3'-OH csoportjának oxigénatomja a 3'-illesztési helyhez kötődik, amikor a két exon kapcsolódik és az intron felszabadul. Az intront áramvonalas alakzatba hozzák, úgynevezett lárvává, amelyet ezután lebontanak.
Ezzel szemben a spliciceosomák nem játszanak szerepet az ön-splicingban. Itt az intronokat magát az RNS szekunder szerkezete zárja ki a transzlációból. A tRNS enzimatikus splicingja (transzfer RNS) eukariótákban és archeákban fordul elő, baktériumokban azonban nem.
Az illesztési folyamatnak a lehető legnagyobb pontossággal az exon-intron határon meg kell történnie, mivel csak egyetlen nukleotiddal történő eltérés az aminosavak helytelen kódolásához vezet, és ezáltal teljesen különböző fehérjék képződéséhez vezet.
Egy pre-mRNS splicingje másképp fordulhat elő a környezeti hatások vagy a szövettípus miatt. Ez azt jelenti, hogy ugyanazon DNS-szekvenciából és így ugyanazon pre-mRNS-ből különböző fehérjék képződhetnek. Ezt a folyamatot alternatív illesztésnek nevezik. Az emberi sejt körülbelül 20 000 gént tartalmaz, de többszázezer fehérjét képes előállítani az alternatív illesztések miatt. Az összes emberi gén körülbelül 30% -ának van alternatív splicingje.
Az összeillesztés nagy szerepet játszott az evolúcióban. Az exonok gyakran a fehérjék egyes doméneit kódolják, amelyek különböző módon kombinálhatók egymással. Ez azt jelenti, hogy nagyon sokféle, teljesen eltérő funkciójú fehérjék állíthatók elő néhány exonból. Ezt a folyamatot exon shufflingnak hívják.
Betegségek és betegségek
Néhány örökletes betegség szorosan összekapcsolható a splicingnel. A nem kódoló intronok mutációi általában nem vezetnek hibákhoz a fehérjék képződésében. Ha azonban mutáció történik egy intrón olyan részén, amely fontos a splicing szabályozásához, ez az pre-mRNS hibás splicingéhez vezethet. A kapott érett mRNS ezután hibás, vagy a legrosszabb esetben káros fehérjéket kódol. Ez a helyzet például a béta-talasémia bizonyos típusai esetében, az öröklött vérszegénység esetén. Az ilyen módon kialakuló betegségek egyéb képviselői például az Ehlers-Danlos szindróma (EDS) II típusú és a gerincizom atrófiája.



.jpg)